Manejo de la inestabilidad anterior de hombro con defectos óseos
Management of anterior instability of the shoulder with bone defects
Resumen:
Objetivo: el objetivo del presente artículo de revisión es resumir la información más relevante acerca de la inestabilidad de hombro con defectos óseos y servir de guía para el estudio de esta patología y su manejo.
Método: revisión de la literatura.
Resultado y conclusiones: el estudio de la inestabilidad con defecto óseo implica una correcta detección clínica y radiológica. La tomografía computarizada con reconstrucción 3D puede proporcionar un análisis preoperatorio objetivo de la ubicación y el grado del defecto, y la artroscopia diagnóstica juega un papel importante en la toma de decisiones de tratamiento. La definición de los defectos óseos de la glena, defectos humerales y los defectos óseos combinados, conjuntamente con el concepto del glenoid track, son fundamentales para la adecuada comprensión del riesgo de recidiva y la posición relativa glenohumeral para que esta se produzca, justificando así el uso de técnicas de bloque óseo asociadas a la reparación de tejidos blandos. Es objeto de debate el porcentaje de defecto de la glena crítico para justificar la necesidad de aplicar estas técnicas. El procedimiento de Latarjet y otras técnicas de bloque óseo se usan ampliamente para tratar defectos óseos glenoideos. Para los defectos óseos humerales, el remplissage es una técnica ampliamente utilizada, destacando el conocimiento de la posible influencia que puede tener sobre el rango de movimiento postoperatorio.
Relevancia clínica: las recomendaciones planteadas en este artículo pretenden servir de soporte para el estudio y la toma de decisiones en la práctica clínica de especialistas que se enfrenten a esta patología.
Abstract:
Objective: A review is made to summarize the most relevant information on shoulder instability with bone defects and to serve as a guide for the study of this type of disorder and its management.
Method: A literature review was carried out.
Results and conclusions: The study of instability with bone defects requires correct clinical and radiological detection. Computed tomography with three-dimensional reconstruction can offer an objective preoperative analysis of the location and degree of the defect, and diagnostic arthroscopy plays an important role in deciding treatment. The definition of bone defects of the glenoid cavity, humeral defects and combined bone defects, together with the glenoid track concept, are fundamental for a correct understanding of the risk of relapse and the relative glenohumeral position in which the latter occurs - thus warranting the use of bone block techniques associated to soft tissue repair. The critical percentage glenoid cavity defect justifying the need to apply these techniques is subject to debate. The Latarjet procedure and other bone block techniques are widely used to treat glenoid bone defects. In the case of humeral bone defects, remplissage is a widely used procedure, and may exert an influence upon the postoperative range of motion.
Clinical relevance: The recommendations made in this article seek to serve as a support for study and decision making in the clinical practice of specialists that deal with disorders of this kind.
Introducción
La interacción coordinada entre estructuras estáticas, dinámicas y óseas es necesaria para mantener la cabeza humeral centrada en la glena en todas las posiciones de la mano en el espacio(1,2). La inestabilidad puede ser el resultado tanto de la alteración de los estabilizadores estáticos (labrum, cápsula y ligamentos glenohumerales) como de los estabilizadores dinámicos (musculatura del manguito de los rotadores), con la consecuente alteración de la anatomía articular. Tras una luxación traumática inicial, la patología más frecuente es la avulsión capsulolabral anteroinferior con o sin atenuación del ligamento glenohumeral asociada correspondiente(3,4).
Se han descrito varios factores que afectan las tasas de recurrencia, incluyendo: edad del paciente, tipo de luxación, deportes de contacto, hiperlaxitud y defecto óseo significativo(5,6). Los defectos óseos por impactación posterosuperior de la cabeza del húmero o la pérdida de hueso glenoideo anteroinferior juegan un papel importante en la inestabilidad glenohumeral anterior, al alterar el área de contacto articular, su congruencia y la función de los componentes de restricción estáticos(7,8,9,10). El estudio de los defectos óseos y su relación con la inestabilidad ha sido un tema ampliamente discutido en la literatura. Burkhart y De Beer(10) en su estudio han descrito el papel contribuyente de los defectos óseos en la inestabilidad de hombro, destacando su papel en el fracaso de procedimientos de estabilización artroscópica y reportando un 67% de recidivas. Definen el término engaging Hill-Sachs y recomiendan que los pacientes en los que se identifique no deben ser tratados con técnicas artroscópicas de partes blandas.
Varios estudios permiten entender la relación de los defectos óseos bipolares humeral y glenoideo, y su implicación en la luxación recidivante: Yamamoto et al.(11) y su concepto de glenoid track (GT), en el que relaciona el tamaño y la ubicación del defecto humeral y glenoideo, y su implicación en la inestabilidad mediante estudio en cadáver. Más recientemente, Di Giacomo, Itoi y Burkhart(12), con su descripción de la lesión de Hill-Sachs y su concepto de lesión on-track/off-track como evolución de la conocida lesión engaging/non-engaging, han permitido comprender estos defectos y valorarlos en la toma de decisiones al tratar este tipo de lesiones.
El manejo de los defectos óseos en la inestabilidad del hombro ha sido un desafío para los cirujanos durante muchos años. Se ha demostrado que algunos procedimientos no anatómicos previenen la luxación recidivante, pero pueden estar asociados con rigidez y artrosis(13).
El objetivo de esta revisión narrativa de la literatura es resumir la información más relevante acerca de la inestabilidad anterior de hombro con defectos óseos asociados y servir de guía para el estudio de esta patología y su manejo.
Relevancia de los defectos óseos glenoideos
Aunque los defectos glenoideos están presentes en solo el 22% de los pacientes con luxaciones agudas, se ha reportado en el 49 al 86% de los pacientes con luxación recidivante(1,14,15,16,17,18). La pérdida ósea glenoidea y la reabsorción de fragmentos conduce a una alteración de la forma de la glena descrita como en forma de pera invertida(10,19,20). La deficiencia anteroinferior del hueso glenoideo altera la capacidad de mantener la cabeza humeral centrada en el rango articular, lo que conduce a una disminución de la resistencia a la luxación anterior de la cabeza del húmero.
Con una cantidad “significativa” de defecto, la cabeza del húmero puede dislocarse anteriormente con solo una cantidad mínima de traslación. Se ha debatido mucho sobre cómo cuantificar la pérdida ósea anterior y cuánta pérdida ósea se necesita para considerar un defecto significativo. Burkhart y DeBeer(10) encontraron una tasa de recurrencia del 4% después de la reparación artroscópica de Bankart sin la presencia de defectos óseos significativos (más del 25% de pérdida de diámetro glenoideo inferior o lesión de Hill-Sachs enganchada) y una tasa de inestabilidad recurrente del 67% en atletas con defectos significativos (más del 25% de pérdida del diámetro glenoideo inferior o lesión de Hill-Sachs enganchada)
Gerber y Nyffeler(21) informaron de una pérdida de resistencia superior al 30% a la luxación anterior del hombro cuando la magnitud del defecto anteroinferior era mayor de la mitad del diámetro glenoideo anteroposterior (AP) máximo. Itoi et al.(7) realizaron osteotomías secuenciales en hombros de cadáveres de la cavidad anteroinferior glenoidea y encontraron que la estabilidad al realizar una traslación anterior fue significativamente menor con un defecto óseo mayor del 21% del diámetro de la glena. Otros estudios han demostrado también que un defecto glenoideo ≥ 25% del ancho glenoideo causa inestabilidad incluso después de la reparación de Bankart, mientras que un defecto ≤ 17,5% no causa inestabilidad(22). Se ha demostrado que el aumento del tamaño del defecto óseo glenoideo se correlaciona con disminución de la estabilidad de la articulación glenohumeral(21,23), aunque no hay acuerdo sobre la cantidad exacta de pérdida ósea necesaria para considerar una lesión significativa.
Una posible explicación para esta falta de acuerdo es que estos estudios biomecánicos originales investigaron defectos glenoideos aislados, mientras que hoy se sabe que la mayoría de los pacientes con luxación anterior recidivante tienen defectos combinados de la cabeza humeral y la glena(24).
Otros estudios biomecánicos más recientes que examinan defectos óseos combinados han revelado una disminución significativa en la estabilidad glenohumeral con defectos glenoideos tan pequeños como 10 a 15% del ancho glenoideo(25,26).
Más recientemente se ha descrito el concepto de defectos subcríticos, en el cual un porcentaje menor de defecto óseo tras una reparación de Bankart no necesariamente resulta en un nuevo episodio de luxación, pero sí puede producir un peor resultado funcional en escalas clínicas del paciente al comparar los casos de reparación exclusiva de partes blandas con aquellos pacientes tratados con técnica de aumentación ósea. Reportan así que defectos mayores del 13,5% conducen a una disminución clínicamente significativa en las puntuaciones del índice Western Ontario Shoulder Instability (WOSI) consistentes con resultados desfavorables, incluso en pacientes que no sufren nuevos episodios de luxación(27).
Relevancia de los defectos óseos humerales
Las lesiones de Hill-Sachs implican un defecto de impactación en la cabeza humeral posterolateral cuando la cabeza humeral entra en contacto con el borde glenoideo anteroinferior durante una luxación anterior del hombro. Está presente aproximadamente en un 47% de los casos de primera luxación glenohumeral anterior y hasta en un 90% de los casos recurrentes(15), estableciéndose además una correlación directa entre la gravedad de los defectos óseos y el número de episodios de luxación recidivante(8,18,28).
Las lesiones menores del 20% de la circunferencia de la cabeza humeral generalmente no son causa significativa de inestabilidad(2,14). Las lesiones mayores del 40% se consideran grandes y se correlacionan con una mayor probabilidad de luxación recurrente(2,18). Los defectos entre el 20 y el 40% pueden ser importantes, pero dependen de la ubicación, la orientación y el recorrido respecto a la glena anteroinferior.
No solo la ubicación de la lesión de Hill-Sachs, sino también su orientación, parecen afectar al riesgo de producir luxación recurrente del hombro. Burkhart y De Beer(10) definen una lesión de Hill-Sachs enganchante como aquella en la que se presenta el eje más largo de la lesión de Hill-Sachs paralelo a la glena anterior con la extremidad en posición funcional de abducción y rotación externa. Aunque es difícil establecer una definición adecuada del término enganchante y su uso puede llevar a errores porque pueden existir diferencias interobservador en su valoración por distintos cirujanos, los autores reportan que, en presencia de esta lesión, las reparaciones con gestos sobre partes blandas exclusivamente tienen una tasa elevada de fracaso. Explican además que una lesión enganchante era creada con la extremidad en abducción y rotación externa, mientras que una lesión no enganchante se crea con la extremidad en aducción.
Cho et al.(29) cuantificaron la orientación de la lesión de Hill-Sachs midiendo el ángulo de Hill-Sachs, entre el eje longitudinal de la diáfisis humeral y el eje de la porción más profunda de la lesión de Hill-Sachs en el plano frontal en tomografía computarizada (TC) en 3 dimensiones (3D). Reportaron así que el ángulo de Hill-Sachs promedio fue de 25,6° para Hill-Sachs enganchante y de 13,8° para lesión no enganchante.
Di Giacomo et al.(30) también miden la orientación de la lesión de Hill-Sachs y dividen a los pacientes en 2 grupos: aquellos en los que la luxación inicial ocurre con la extremidad a menos de 60° de abducción (grupo ADD) y aquellos en los que ocurre con la extremidad a más de 60° (grupo ABD). El ángulo de Hill-Sachs fue de 32,4° en el grupo ABD y de 16,1° en el grupo ADD. En su serie, los autores especulan que la lesión de Hill-Sachs en el grupo ABD tenía más probabilidad de engancharse porque era más paralela a la glena anterior con la extremidad en posición funcional. La orientación de la lesión de Hill-Sachs venía determinada por la posición de la extremidad al crearse la lesión y, si es paralela a la glena con la extremidad en posición funcional, es más probable que se enganche.
En otro estudio biomecánico, Kawakami et al.(31), en un intento de especificar la posición de la extremidad cuando se crea la lesión de Hill-Sachs, describen que la posición del brazo en la que mejor se ajustan el Hill-Sachs y el borde glenoideo anterior es a 74° de abducción, 27° de rotación externa y 3° de flexión horizontal, que parece ser la posición cuando se creó la lesión de Hill-Sachs. Con este resultado, sugieren 2 posibilidades: la luxación se produjo en esta posición o la lesión de Hill-Sachs no se creó en el momento de la luxación, sino más tarde en el rango de movimiento. Así, este estudio nos da una mejor comprensión del momento en el que ocurre la lesión de Hill-Sachs.
Defectos combinados y concepto de glenoid track
Las lesiones óseas de la glena y del húmero son muy comunes en pacientes con inestabilidad anterior del hombro. Aproximadamente, el 80% de ellos tienen ambas lesiones al mismo tiempo, lo que se denomina lesión bipolar. Como ha sido mencionado, estudios biomecánicos han demostrado que un defecto glenoideo ≥ 25% del ancho glenoideo causa inestabilidad incluso después de la reparación de Bankart, mientras que un defecto ≤ 17,5% no suele ser causa de inestabilidad(32). El rango entre 17,5 y 25% se ha referido como una “zona gris”, llamada pérdida ósea subcrítica(33). El riesgo de causar inestabilidad de una lesión de Hill-Sachs no solo depende de sí misma, sino también del tamaño del defecto en la glena. Para evaluar estas lesiones en conjunto, se introdujo el concepto de GT.
Yamamoto et al.(34), en su estudio en cadáver, describen que, con el brazo en rotación externa máxima, extensión horizontal e incrementos de la elevación de la extremidad (0, 30 y 60° de abducción), el contacto de la glena cambia de la porción inferomedial a la superolateral de la porción posterior de la cabeza humeral, creando una zona de contacto que llamaron glenoid track. El margen medial del GT se localiza 18,4 ± 2,5 mm medial a la huella del manguito rotador, lo que es equivalente al 84 ± 14% del diámetro de la glena. Reportan así que una lesión de Hill-Sachs tiene mayor riesgo de engancharse si se extiende sobre el margen medial del GT.
El ancho del GT disminuye si hay un defecto óseo glenoideo. Así, los defectos óseos glenoideos y de la cabeza humeral pueden evaluarse uno con respecto al otro. Si el margen medial de una lesión de Hill-Sachs está dentro del GT, hay soporte óseo adyacente a la lesión de Hill-Sachs y la lesión de Hill-Sachs estará on-track; si el margen medial de la lesión de Hill-Sachs es más medial que el GT, no hay soporte óseo y la lesión de Hill-Sachs será off-track(12). En el siguiente apartado se define con claridad la metodología para el cálculo del GT.
Evaluación de los defectos óseos
Evaluación radiológica
El defecto óseo puede evaluarse con radiografías simples, TC, resonancia magnética (RM) e intraoperatoriamente mediante artroscopia.
El estudio radiológico incluye una vista AP y de perfil de la escápula y axilar, que confirman la dirección de la luxación y los defectos óseos asociados o fracturas. La proyección de Stryker notch destaca la zona posterolateral de la cabeza humeral, pudiendo identificar defectos óseos a este nivel, y la proyección de West Point valora específicamente la pérdida de hueso glenoideo, como destacan Itoi et al.(35) en su estudio, en el que demuestran una alta correlación con la TC en la estimación del defecto óseo glenoideo.
La TC es la prueba de imagen de elección para evaluar las deficiencias óseas. Las indicaciones para realizarla incluyen aprensión significativa en niveles menores de abducción, inestabilidad con provocación mínima, múltiples episodios de luxación, cirugía de revisión y cualquier defecto óseo detectado en radiografías simples. Existen distintos métodos de medición para el cálculo del tamaño real de la glena y del defecto óseo mediante imágenes preoperatorias de TC en 2 dimensiones (2D) y 3D(16,36), en las que se realiza sustracción digital de la cabeza humeral para obtener una visión completa frontal de la glena(1,37,38).
El margen glenoideo anterior tiene una configuración curva; en el momento en el que empieza a existir pérdida ósea, la línea curva se convierte en recta, siendo este el primer signo de pérdida ósea glenoidea. A medida que avanza el defecto óseo, la línea recta anterior se alarga y, cuando existen grados severos de pérdida ósea, la curva anterior de la glena se vuelve cóncava(36). La comparación de las imágenes de la glena afectada con la contralateral es el método más preciso para el cálculo del defecto óseo glenoideo, ya que existe una simetría casi perfecta entre la forma y el tamaño de ambas fosas glenoideas, siempre que la glena contralateral no haya presentado episodios de luxación glenohumeral(39,40).
Para poder calcular el defecto, se debe obtener una vista frontal de la glena y dibujar 2 líneas. La primera constituye la línea de referencia y se realiza siguiendo el eje largo de la glena desde el tubérculo supraglenoideo hasta la parte más inferior de la glena. La segunda línea se traza en ángulo recto al eje largo de la glena en la mitad inferior, en el punto que corresponde al ancho máximo de la superficie glenoidea. A continuación, se trazan las mismas líneas en el hombro contralateral para utilizar la glena sana como guía del tamaño y la configuración, pudiendo determinar el grado de pérdida ósea con exactitud(41).
La RM también se ha descrito como herramienta para medir defectos óseos glenoideos, permitiendo disminuir la irradiación al paciente y estudiar lesiones asociadas. El método de medición más extendido es el publicado por Sugaya et al., en el que se mide el diámetro de la glena mediante el best fit circle, dibujando un círculo que se adapta a la circunferencia de la glena y ajustándolo en el borde inferior(42); sin embargo, la estimación de la pérdida ósea en la parte anterior de la glena basada en el margen posterior puede sobrestimar hasta un 5% el defecto, ya que existen diferencias entre el contorno anterior y posterior de la glena, siendo mayor la sobrestimación si el defecto óseo es moderado o severo(43). A pesar de esto, se ha descrito que su cuantificación se compara favorablemente con mediciones obtenidas con TC y TC en 3D; se relaciona su precisión con el nivel de entrenamiento, requiriendo superar una curva de aprendizaje para manejar la técnica(44).
En la actualidad, hay varios métodos disponibles para evaluar y cuantificar la lesión de Hill-Sachs. La medición de la longitud, el ancho y la profundidad en las reconstrucciones de TC ha demostrado fuertes coeficientes de correlación inter- e intraobservador en la literatura(45). Se ha descrito que las lesiones más grandes y orientadas más perpendicularmente al eje humeral tienen más probabilidad de ser enganchantes(29). La TC en 3D es el gold standard para la evaluación de la lesión de Hill-Sachs; sin embargo, algunos estudios han comunicado no encontrar diferencias significativas entre las mediciones de TC en 3D y RM en 3D, reportando así que la dosis de radiación asociada a la TC podría potencialmente evitarse(46).
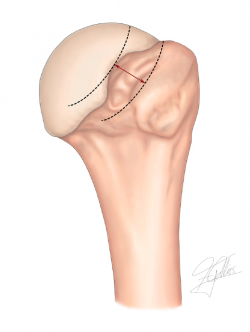
La deformidad de Hill-Sachs se mide mejor en los cortes axiales en la cara más superior del húmero proximal, por encima de la apófisis coracoides(47). La región más ancha de la deformidad de Hill-Sachs constituye la medida más importante respecto a la trayectoria glenoidea y la profundidad de la deformidad se puede estudiar dibujando un círculo a través de la cara superior del húmero proximal(41).
El cálculo del GT permite determinar la probabilidad de que la lesión de Hill-Sachs se enganche en el borde anteroinferior de la glena, siendo una herramienta útil a la hora de planificar la cirugía(45,48). Su valoración es importante, entre otras cosas, porque puede modificar la elección del tratamiento y el gesto quirúrgico a realizar, pudiendo ser necesario asociar en lesiones off-track la técnica de remplissage o procedimientos de tope óseo, dependiendo del tamaño del defecto glenoideo y el riesgo de recurrencia.
Cálculo del glenoid track
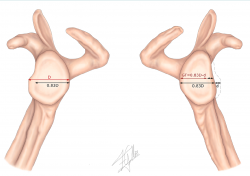
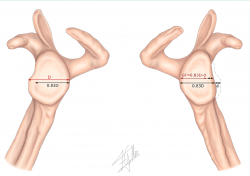
Para poder clasificar una lesión de Hill-Sachs en on-track u off-track, se deben realizar los siguientes pasos (Figuras 1 y 2):
1. Medición del diámetro real de la glena (D).
2. Medición del defecto óseo glenoideo (d).
Para poder calcularlos se pueden utilizar las mediciones descritas previamente en la TC comparándolas con el hombro contralateral o mediante la medición del best fit circle en el corte sagital de la RM.
3. Cálculo del GT en función de la siguiente fórmula: 0,83 × (D − d).
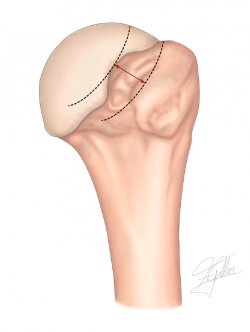
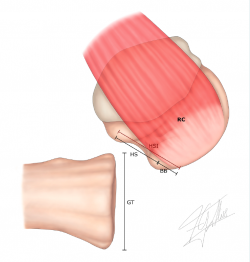
4. Medición del ancho del intervalo Hill-Sachs (HIS) (Figura 3): es el resultado de la medición del ancho del Hill-Sachs (HS) más el puente óseo o bone bridge (BB) entre el borde medial de la inserción del manguito y la región lateral de la lesión del Hill-Sachs(49) (HIS = HS + BB).
reaca.28373.fs2007039-figura3.png
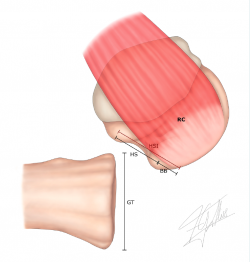
Figura 3. Medición del intervalo Hill-Sachs (HSI): es el resultado de la medición del ancho del Hill-Sachs (HS) más el puente óseo o bone bridge (BB) entre el borde medial de la inserción del manguito y la región lateral de la lesión del Hill-Sachs: HSI = HS + BB. RC: inserción del manguito rotador.
Tras realizar los cálculos descritos previamente, podemos encontrar 2 situaciones:
1. GT > HIS: lesión on-track. La totalidad de la lesión se encuentra dentro del GT y no se “engancha” en la glena al realizar los movimientos más extremos.
2. GT < HIS: lesión off-track. Parte de la lesión sobresale del GT, enganchándose en el borde anteroinferior de la glena en los movimientos más extremos.
Aunque se ha observado un alto nivel de concordancia interobservador (> 90%) a la hora de la evaluación del defecto glenoideo, algunas publicaciones destacan que puede existir una alta variabilidad en la utilización del borde medial de la inserción del manguito y los márgenes del defecto de Hill-Sachs para el cálculo del ancho del intervalo Hill-Sachs condicionando la medición del GT y el algoritmo de tratamiento(50,51). Esta variabilidad se aprecia principalmente en imágenes bidimensionales y es más evidente en las imágenes de RM que en la TC(40).
En un intento de clarificar la existencia de defectos óseos subcríticos en la lesión de Hill-Sachs y su influencia sobre los resultados en las escalas de valoración postoperatorias, Yamamoto et al. en su estudio dividen el GT en 4 zonas, basándose en la medición del porcentaje de “ocupación de Hill-Sachs” en TC en 3D. Reporta así que los pacientes con lesiones on-track pueden dividirse en 2 subgrupos: aquellos con un porcentaje de ocupación de Hill-Sachs ≥ 75% (lesión del track periférica), que mostraron un resultado funcional significativamente peor aun sin nuevos episodios de luxación, comparados con aquellos con un porcentaje de ocupación < 75% (lesión del track central)(52).
Evaluación artroscópica
Un defecto óseo glenohumeral significativo se puede identificar durante la artroscopia buscando la forma de “pera invertida” de la glena (más del 25% de pérdida del diámetro glenoideo inferior) o evaluando el recorrido de la lesión de Hill-Sachs(10). Durante la artroscopia diagnóstica, se puede retirar la tracción y evaluar el rango de movimiento con flexión, abducción y rotación externa progresiva. Si la cabeza del húmero cae en el defecto glenoideo anteroinferior con el brazo en posición de abducción y rotación externa, hay una lesión de Hill-Sachs enganchante o lesión bipolar off-track.
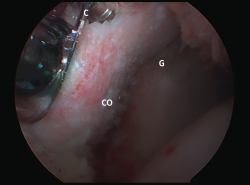
Para evaluar el defecto óseo glenoideo artroscópicamente, con la cámara en el portal anterosuperior, se miden las distancias desde la cavidad glenoidea posterior hasta el área desnuda y desde el área desnuda hasta el borde anterior. En el margen articular en la porción inferior de la glena, los bordes anterior y posterior son equidistantes del área central desnuda; por lo tanto, para calcular el defecto se asume que este mide la diferencia entre ambos. Para hacerlo constar como porcentaje, se divide el defecto entre el doble de la distancia del área desnuda al borde posterior(53) (Figura 4).
Técnicas para el manejo del defecto óseo glenoideo (Tabla 1)
Procedimiento de Bristow
Descrito por Helfet en 1958 en nombre de su mentor Rowley Bristow, de Sudáfrica, consiste en usar la punta de la coracoides, distal a la inserción del pectoral menor, dejando así insertado el tendón conjunto en la porción de coracoides transferida, y pasarla a través de una incisión en el subescapular para colocarla en la parte inferior de la glena(54). En esta técnica, la coracoides se coloca orientándola a través de la cara donde se ha realizado la osteotomía. Helfet originalmente no utilizaba el tornillo en su técnica y únicamente suturaba el fragmento a la pared muscular anterior. En 1964, fue modificada por Mead y Sweeney(55) para incluir fijación interna rígida.
Procedimiento de Latarjet
Se trata de un procedimiento de uso ampliamente extendido para el tratamiento de los defectos óseos de la glena en la inestabilidad de hombro, mediante técnica abierta, mini-open o artroscópica(56,57,58). Latarjet, en 1954(59), describió la técnica de bloque óseo de coracoides, sugiriendo que la porción horizontal de la misma fuera fijada con un tornillo a ras del margen anteroinferior de la glena, mediante una incisión horizontal a través de las fibras del subescapular. May(60) explicó que la eficiencia de la técnica era atribuible al efecto de hamaca que jugaba el tendón coracobíceps y el tendón del subescapular en abducción-rotación externa, más que el tope óseo en sí.
Patte(61) propuso el término triple cerrojo para describir la eficacia de la técnica:
1. Efecto óseo gracias a la fijación estable con tornillo del bloque óseo coracoideo, plano sobre una posición subecuatorial, a ras del margen anterior de la glena.
2. Efecto hamaca por la preservación de las fibras musculotendinosas del tercio inferior del subescapular.
3. Efecto de reparación capsular con la sutura del flap capsular lateral al ligamento coracoacromial remanente insertado en la coracoides.
Es un procedimiento ampliamente utilizado y los resultados reportados son muy satisfactorios(62). Burkhart et al.(9) comunicaron los resultados de 102 pacientes tratados con el procedimiento Latarjet modificado para pérdida ósea glenoidea superior al 25%. El 4% de los pacientes sufrió una luxación recurrente, el 5% tuvo quejas de inestabilidad y hubo una pérdida promedio de 5° de rotación externa con el brazo en aducción. Allain et al.(63) informaron sobre 56 pacientes seguidos durante un promedio de 14 años después del procedimiento de Latarjet. No tuvieron recidivas de luxaciones y el 12% de los pacientes se quejaron de inestabilidad recurrente. Hovelius et al.(64) informaron un seguimiento a largo plazo de más de 10 años después del procedimiento Bristow-Latarjet con una fusión del 83% de la coracoides, 5% de reluxación y 1% de cirugía de revisión.
Se han descrito resultados satisfactorios y alta efectividad de este procedimiento en jugadores de fútbol(65) y jugadores de rugby(66). También se han descrito buenos resultados para restaurar con éxito la estabilidad del hombro en pacientes de edad avanzada(67) y al ser utilizado en cirugía de revisión(68). Más recientemente, se han informado los resultados del procedimiento de Latarjet artroscópico (Figura 5), con resultados equivalentes a los del procedimiento abierto, aunque es claramente más exigente desde el punto de vista técnico(57,69).
Técnicas de aporte de injerto óseo glenoideo aislado
Estas alternativas implican el uso de injerto óseo de cresta ilíaca para la reconstrucción(70) mediante técnicas de bloque óseo, como modificaciones de la técnica de Eden-Hybinette(71) o el J graft procedure(72), y técnicas de reconstrucción mediante el uso de injerto de tibia distal(73).
Técnica de Eden-Hybinette
Descrita en 1918 por Eden y en 1932 por Hybinette, usa un injerto de cresta ilíaca para la aumentación ósea glenoidea. De su variante artroscópica, descrita inicialmente por Taverna et al.(74), se han descrito múltiples modificaciones. Una de ellas, descrita por Boileau et al.(75), se indica como rescate de pacientes con fracaso de Latarjet previo mediante el uso de injerto de cresta ilíaca ipsilateral tricortical. Tras regularizar su porción cortical, se realiza un agujero con broca de 2,8 mm pasando las suturas guía. Se prepara la glena mediante el uso de guía específica y brocado para posteriormente recuperar la pastilla ósea con suturas guía. Se fija entonces el injerto con el sistema de suspensión y botón anterior y posterior en la glena. Reportan en su estudio resultados satisfactorios en escalas de valoración clínica y sin complicaciones o necesidad de reintervenciones.
J graft procedure
Técnica abierta en la que se utiliza un injerto óseo bicortical de cresta ilíaca en forma de J que es impactado en la glena en la zona del defecto, previa preparación de la glena. Está descrita para su fijación por impactación, con el uso excepcional de fijación adicional con un tornillo canulado en los casos que lo requieran. Con su uso, los autores reportan resultados satisfactorios en escalas de valoración clínica y también una pérdida de rotación externa de 4,36° en aducción y de 3,19 a 90° de abducción. Sin recurrencias de inestabilidad y con 1 fractura traumática del injerto(72).
El interés en eliminar los implantes metálicos para la fijación del injerto ha impulsado el desarrollo de técnicas artroscópicas sin su uso. Ejemplos de estas técnicas, además del citado J graft procedure, son la descrita por Hachem et al.(76), con el uso de cerclajes con suturas de alta resistencia, la descrita por Zhao et al.(77), con suturas de anclajes en la glena nativa, y la descrita por Whelan et al.(78), con el uso de matriz de dermis humana acelular, entre otras.
Injerto de tibia distal
Descrito para casos de inestabilidad recidivante con al menos un 15% de defecto óseo anterior de la glena, mediante el uso de aloinjerto de tibia distal para la reconstrucción del defecto de la glena. Reportan, con un seguimiento promedio de 45 meses, excelentes resultados clínicos y una mínima reabsorción del injerto(74).
Manejo de la lesión de Hill-Sachs
El principio del tratamiento de la lesión de Hill-Sachs es evitar su encaje con el borde glenoideo anterior. Esto puede lograrse mediante el uso de técnicas anatómicas o técnicas no anatómicas, llenando el defecto de la cabeza humeral. Algunas opciones descritas implican el acortamiento o retensado del tejido blando anterior(79), o la osteotomía rotacional del húmero(80). Entre alternativas de llenado del defecto, se han descrito el llenado de la lesión con un injerto óseo(81) o tejido blando (remplissage)(82) o plastia/corrección percutánea de la cabeza humeral(83,84).
Remplissage
Connolly(85) fue el primero en describir la tenodesis del infraespinoso en el defecto de la cabeza humeral y, posteriormente, Wolf et al.(82) describieron por primera vez la variación artroscópica de la técnica, aplicándola en combinación con la reparación de Bankart, y a la que denominaron remplissage. La técnica consiste en rellenar el defecto de la cabeza humeral mediante la capsulotenodesis del tendón del infraespinoso y la cápsula glenohumeral. Los resultados de la técnica original(86) y su modificación(87) han sido reportados y, debido a su sencillez, se ha vuelto popular y ampliamente utilizada.
Desde su descripción, se han publicado excelentes resultados funcionales con su uso en la inestabilidad recurrente, con el inconveniente de una variedad de repercusiones reportadas sobre el rango de movilidad postoperatoria. Cuando se compara con la reparación de Bankart aislada, se ha descrito que evita el 20% de recurrencia reportado en estos casos, sin diferencias significativas en cuanto a restricciones de movilidad resultante(88,89).
Estudios biomecánicos como el de Elkinson et al.(90) han reportado una limitación resultante de la rotación externa en aducción y abducción de 14,5 y 6,2°, respectivamente. Boileau et al.(91) también reportaron una restricción en la rotación externa tras el remplissage de 8° en aducción y 9° en abducción en su serie, con un 90% de retorno a la actividad deportiva y un 68% a nivel prelesional.
Injerto óseo humeral
El aloinjerto de la cabeza humeral, más comúnmente utilizado en el contexto de grandes lesiones de Hill-Sachs debido a la inestabilidad, ha mostrado mejoras significativas en el rango de movilidad y en las puntuaciones de la American Shoulder and Elbow Surgeons (ASES) hasta un año después de la operación. Las tasas de reincorporación al trabajo y los niveles de satisfacción reportados son altos después de la intervención. Sin embargo, las tasas de complicaciones (entre 20 y 30%), como la reabsorción y la necrosis del injerto, y la artrosis, y la tasa de reintervenciones reportadas (26,67%) son relevantes(81).
Alternativas terapéuticas en el manejo de los defectos óseos
Una correcta interpretación del defecto óseo y del GT, añadiendo factores predictivos (edad, sexo, actividad deportiva(9), lesiones concomitantes, etc.), debe ser manejada para la decisión terapéutica.
En un intento de predecir preoperatoriamente el éxito o el fracaso con la reparación aislada de partes blandas, Balg y Boileau publicaron el Instability Severity Index Score (ISIS)(92). Se basa en un cuestionario preoperatorio, examen clínico y revisión de radiografías. Aquellos pacientes con una puntuación mayor de 6 puntos tuvieron una tasa de recurrencia del 70% con reparación de partes blandas sola y, en ellos, recomiendan un procedimiento asociado para abordar el defecto óseo, siendo insuficiente el Bankart artroscópico aislado.
El uso de esta escala de valoración ha sido objeto de debate en la literatura y existen autores que han reportado que, en pacientes con inestabilidad anterior en los que se plantea una reparación de Bankart con puntuaciones ≤ 6, no es capaz de predecir el aumento del riesgo de recidiva a medio plazo. Así, explican que su eficacia para definir un riesgo preoperatorio aumentado de recurrencia después de una reparación de Bankart es limitada en poblaciones de bajo riesgo(93).
En un estudio reciente, Di Giacomo et al.(94) reportan resultados prometedores con su modificación de la escala ISIS, incorporando el concepto de GT, a la que llaman Glenoid Track Instability Management Score (GTIMS). Comunican así que dicha modificación de la escala, al utilizar estudios de imagen avanzada y el principio de on/off-track, permite delimitar de forma más conservadora el tratamiento de la inestabilidad anterior con resultados postoperatorios prometedores. En general, reportan diferencias mínimas en los resultados entre los pacientes que ambas escalas indican para abordar el defecto óseo de glena; sin embargo, reportan mejores resultados en pacientes indicados para la reparación artroscópica de Bankart de acuerdo con el GTIMS.
Esquema de manejo quirúrgico (Tabla 2)
Aunque, como se ha mencionado anteriormente, es motivo de debate el porcentaje de defecto significativo para la toma de decisiones en el manejo quirúrgico de los defectos óseos glenohumerales, resumimos a continuación datos ampliamente aceptados en la literatura para el manejo de estas lesiones.
La reparación artroscópica de partes blandas aislada (reparación de Bankart) está indicada en presencia de una lesión de Hill-Sachs on-track no enganchante y pérdida ósea glenoidea inferior al 20-25%.
Pacientes con defecto de glena < 25% y lesión de Hill-Sachs mayor del 30% u off-track pueden ser tratados con una reparación de partes blandas (reparación de Bankart) asociando la técnica de remplissage.
Para el grupo de pacientes con una pérdida ósea glenoidea anteroinferior del 25% o más y una lesión de Hill-Sachs on-track, se recomienda realizar un procedimiento con injerto óseo para aumentar el arco articular glenohumeral, como el procedimiento de Latarjet(10,12,18,95,96,97).
En los pacientes con pérdida ósea glenoidea anteroinferior del 25% o más y una lesión de Hill-Sachs enganchante u off-track, se recomienda el procedimiento de bloque óseo más algún procedimiento que aborde el defecto humeral, como el remplissage o injertos óseos, dependiendo del tamaño y la localización del defecto(12,13,98,99,100,101).
Conclusiones
Los defectos óseos se observan frecuentemente en la inestabilidad anterior. La exploración física y los estudios de imagen como radiografía, TC y RM, en especial la TC con reconstrucción en 3D, pueden proporcionar un análisis preoperatorio objetivo de la ubicación y el grado del defecto, lo cual, sumado a la artroscopia diagnóstica, juega un papel importante en la toma de decisiones del tratamiento. El valor determinante de un defecto significativo de la glena aún es objeto de debate y, aunque inicialmente era aceptado que a partir de defectos mayores del 20-25% se puede relacionar con fracasos de tratamientos exclusivos de partes blandas, más recientemente se han descrito resultados desfavorables con menor porcentaje de defecto óseo glenoideo, siendo necesarios más estudios futuros para determinar estos límites y obtener consensos. La lesión de Hill-Sachs debe evaluarse conjuntamente con la lesión glenoidea, siendo el GT una herramienta útil para evaluar el encaje de estas lesiones bipolares. El procedimiento de Latarjet se usa ampliamente para defectos óseos glenoideos, además de otros procedimientos de bloque óseo descritos en la literatura, y, dado que proporcionan un aumento de la estabilidad del hombro en comparación con el hombro normal, pueden ser una buena indicación para el tratamiento de los atletas de deportes de contacto. Para los defectos óseos humerales enganchantes o combinados con defectos glenoideos, el remplissage es una técnica ampliamente utilizada, destacando el conocimiento de la posible afectación que puede tener sobre la rotación externa en el rango de movimiento postoperatorio.
Figuras
Figura 1. Evaluación de la inestabilidad con defecto óseo. Esquema de medición del diámetro real de la glena contralateral (D) y del defecto óseo glenoideo (d) para el cálculo del glenoid track en función de la siguiente fórmula: 0,83 × (D − d).
Figura 3. Medición del intervalo Hill-Sachs (HSI): es el resultado de la medición del ancho del Hill-Sachs (HS) más el puente óseo o bone bridge (BB) entre el borde medial de la inserción del manguito y la región lateral de la lesión del Hill-Sachs: HSI = HS + BB. RC: inserción del manguito rotador.
Figura 4. Visión de la glena desde el portal anterosuperior. Medición artroscópica del defecto óseo de la glena. Radio posterior: A (mm). Diámetro de la glena = 2A. Medición anterior: B (mm). Defecto: A − B = d mm (pérdida ósea). Porcentaje de defecto: d / 2A = D%.
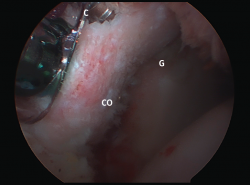
Figura 5. Procedimiento de Latarjet, técnica artroscópica. Visión de la fijación artroscópica de la coracoides (CO) desde el portal J. C: cánula guía para posicionar los tornillos; G: parte anteroinferior de la glena.
Tablas
Información del artículo
Cita bibliográfica
Autores
León Ezagüi
Hospital El Pilar. Grupo Quirónsalud. Barcelona
Luca Baggio
Unidad de Hombro y Codo. Servicio de Cirugía Ortopédica y Traumatología. MC Mutual. Barcelona
María Brotat Rodríguez
Unidad de Hombro y Codo. Hospital Universitario Infanta Elena. Valdemoro, Madrid
Servicio de Cirugía Ortopédica y Traumatología. HU Infanta Elena. Valdemoro. Madrid
Abel Gómez Cáceres
Instituto Malagueño de Traumatología Deportiva (IMATDE). Málaga
José Carlos Yebra Pareja
Servicio de Cirugia Ortopedica y Traumatología. Hospital Marqués Valdecilla. Santander
Servicio de Cirugia Ortopedica y Traumatología. Hospital Clínica Mompía. Santander
Servicio de Traumatología y Cirugía Ortopédica. Complejo Hospitalario Torrecárdenas. Almería
E. P. Hospital de Poniente. El Ejido, Almería
Responsabilidades éticas
Conflicto de interés. Los autores declaran no tener ningún conflicto de interés.
Financiación. Este trabajo no ha sido financiado.
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad de los datos. Los autores declaran que han seguido los protocolos de su centro de trabajo sobre la publicación de datos de pacientes.
Derecho a la privacidad y consentimiento informado. Los autores declaran que en este artículo no aparecen datos de pacientes.
Agradecimientos
A los revisores participantes de este artículo y a los doctores Miguel García Navlet y Abdul Ilah Hachem por su esfuerzo y su guía.
Grupo Joven de Artroscopia (GJA)
Este artículo ha sido coordinado y realizado en el proyecto del Grupo Joven de Artroscopia (GJA) de la Asociación Española de Artroscopia (AEA).
Referencias bibliográficas
-
1Piasecki DP, Verma NN, Romeo AA, et al. Glenoid bone deficiency in recurrent anterior shoulder instability: diagnosis and management. J Am Acad Orthop Surg. 2009;17:482-93.
-
2Chen AL, Hunt SA, Hawkins RJ, et al. Management of bone loss associated with recurrent anterior glenohumeral instability. Am J Sports Med. 2005;33:912-25.
-
3Rowe CR, Patel D, Southmayd WW. The Bankart procedure: a long-term end-result study. J Bone Joint Surg Am. 1978;60:1-16.
-
4Urayama M, Itoi E, Sashi R, et al. Capsular elongation in shoulders with recurrent anterior dislocation. Quantitative assessment with magnetic resonance arthrography. Am J Sports Med. 2003;31:64-7.
-
5Wang RY, Arciero RA. Treating the athlete with anterior shoulder instability. Clin Sports Med. 2008;27:631-48.
-
6Robinson CM, Howes J, Murdoch H, et al. Functional outcome and risk of recurrent instability after primary traumatic anterior shoulder dislocation in young patients. J Bone Joint Surg Am. 2006;88:2326-36.
-
7Itoi E, Lee SB, Berglund LJ, et al. The effect of a glenoid defect on anteroinferior stability of the shoulder after Bankart repair: a cadaveric study. J Bone Joint Surg Am. 2000;82:35-46.
-
8Lynch JR, Clinton JM, Dewing CB, et al. Treatment of osseous defects associated with anterior shoulder instability. J Shoulder Elbow Surg. 2009;18:317-28.
-
9Burkhart SS, De Beer JF, Barth JR, et al. Results of modified Latarjet reconstruction in patients with anteroinferior instability and significant bone loss. Arthroscopy. 2007;23:1033-41.
-
10Burkhart SS, De Beer JF. Traumatic glenohumeral bone defects and their relationship to failure of arthroscopic Bankart repairs: significance of the inverted-pear glenoid and the humeral engaging Hill-Sachs lesion. Arthroscopy. 2000;16:677-94.
-
11Yamamoto N, Muraki T, Sperling JW, et al. Stabilizing mechanism in bone-grafting of a large glenoid defect. J Bone Joint Surg. 2010;92:2059-66.
-
12Di Giacomo G, Itoi E, Burkhart S. Evolving Concept of Bipolar Bone Loss and the Hill-Sachs Lesion: From “Engaging/Non-Engaging” Lesion to “On-Track/Off-Track” Lesion. Arthroscopy. 2014;30(1):90-8.
-
13Ochoa E Jr, Burkhart SS. Glenohumeral bone defects in the treatment of anterior shoulder instability. Instr Course Lect. 2009;58:323-36.
-
14Taylor DC, Arciero RA. Pathologic changes associated with shoulder dislocations. Arthroscopic and physical examination findings in first-time, traumatic anterior dislocations. Am J Sports Med. 1997;25:306-11.
-
15Calandra JJ, Baker CL, Uribe J. The incidence of Hill-Sachs lesions in initial anterior shoulder dislocations. Arthroscopy. 1989;5:254-7.
-
16Sugaya H, Moriishi J, Dohi M, et al. Glenoid rim morphology in recurrent anterior glenohumeral instability. J Bone Joint Surg Am. 2003;85-A:878-84.
-
17Griffith JF, Antonio GE, Yung PS, et al. Prevalence, pattern, and spectrum of glenoid bone loss in anterior shoulder dislocation: CT analysis of 218 patients. AJR Am J Roentgenol. 2008;190:1247-54.
-
18Boileau P, Villalba M, Hery JY, et al. Risk factors for recurrence of shoulder instability after arthroscopic Bankart repair. J Bone Joint Surg Am. 2006;88:1755-63.
-
19Lo IK, Parten PM, Burkhart SS. The inverted pear glenoid: an indicator of significant glenoid bone loss. Arthroscopy. 2004;20:169-74.
-
20Burkhart SS, Danaceau SM. Articular arc length mismatch as a cause of failed Bankart repair. Arthroscopy. 2000;16:740-4.
-
21Gerber C, Nyffeler RW. Classification of glenohumeral joint instability. Clin Orthop Relat Res. 2002;400:65-76.
-
22Yamamoto N, Itoi E, Abe H, Kikuchi K. Effect of an Anterior Glenoid Defect on Anterior Shoulder Stability: A Cadaveric Study. Am J Sports Med. 2009;37(5):949-54.
-
23Montgomery WH Jr, Wahl M, Hettrich C, et al. Anteroinferior bone-grafting can restore stability in osseous glenoid defects. J Bone Joint Surg Am. 2005;87(9):1972-7.
-
24Widjaja AB, Tran A, Bailey M, Proper S. Correlation between Bankart and Hill-Sachs lesions in anterior shoulder dislocation. ANZ J Surg. 2006;76:436-8.
-
25Arciero RA, Parrino A, Bernhardson AS, et al. The effect of a combined glenoid and Hill-Sachs defect on glenohumeral stability: a biomechanical cadaveric study using 3-dimensional modeling of 142 patients. Am J Sports Med. 2015;43(6):1422-9.
-
26Gottschalk LJ 4th, Walia P, Patel RM, et al. Stability of the Glenohumeral Joint With Combined Humeral Head and Glenoid Defects: A Cadaveric Study. Am J Sports Med. 2016;44(4):933-40.
-
27Shaha JS, Cook JB, Song DJ, et al. Redefining "Critical" Bone Loss in Shoulder Instability: Functional Outcomes Worsen With "Subcritical" Bone Loss. Am J Sports Med. 2015;43(7):1719-25.
-
28Hintermann B, Gächter A. Arthroscopic findings after shoulder dislocation. Am J Sports Med. 1995;23(5):545-51.
-
29Cho SH, Cho NS, Rhee YG. Preoperative analysis of the Hill-Sachs lesion in anterior shoulder instability: how to predict engagement of the lesion. Am J Sports Med. 2011;39(11):2389-95.
-
30Di Giacomo G, Golijanin P, Sánchez G, Provencher M. Radiographic analysis of the Hill-Sachs lesion in anteroinferior shoulder instability after first-time dislocations. Arthoscopy. 2016;32:1509-14.
-
31Kawakami J, Yamamoto N, Hatta T, Shinagawa K, Itoi E. In Which Arm Position Is a Hill-Sachs Lesion Created? Am J Sports Med. 2019;47(10):2464-8.
-
32Yamamoto N, Itoi E, Abe H, Kikuchi K. Effect of an Anterior Glenoid Defect on Anterior Shoulder Stability: A Cadaveric Study. Am J Sports Med. 2009;37(5):949-54.
-
33Itoi E, Yamamoto N, Hatta T, Kawakami J. Overview of Evaluation and Management of the Unstable Shoulder With and Without Bone Loss: Definition, Measurement, and Guidelines on Treatment. In: Imhoff A, Savoie III F (eds.). Shoulder Instability Across the Life Span. Berlin: Springer, Heidelberg; 2017.
-
34Yamamoto N, Itoi E, Abe H, et al. Contact between the glenoid and the humeral head in abduction, external rotation, and horizontal extension: a new concept of glenoid track. J Shoulder Elbow Surg. 2007;16:649-56.
-
35Itoi E, Lee SB, Amrami KK, et al. Quantitative assessment of classic anteroinferior bony Bankart lesions by radiography and computed tomography. Am J Sports Med. 2003;31:112-8.
-
36Griffith JF, Antonio GE, Tong CW, Ming CK. Anterior shoulder dislocation: quantification of glenoid bone loss with CT. Am J Roentgenol. 2003;180:1423-30.
-
37Bushnell BD, Creighton RA, Herring MM. Bony instability of the shoulder. Arthroscopy. 2008;24:1061-73.
-
38Chuang TY, Adams CR, Burkhart SS. Use of preoperative three-dimensional computed tomography to quantify glenoid bone loss in shoulder instability. Arthroscopy. 2008;24:376-82.
-
39Shi L, Griffith JF, Huang J, Wang D. Excellent side-to-side symmetry in glenoid size and shape. Skeletal Radiol. 2013;42:1711-5.
-
40Griffith JF, Yung PS, Antonio GE, Tsang PH, Ahuja AT, Chan KM. CT compared with arthroscopy in quantifying glenoid bone loss. AJR Am J Roentgenol. 2007;189:1490-3.
-
41Griffith J. Measuring glenoid and humeral bone loss in shoulder dislocation. Quant Imaging Med Surg. 2019;9(2):134-43.
-
42Sugaya H, Moriishi J, Dohi M, Kon Y, Tsuchiya A. Glenoid rim morphology in recurrent anterior glenohumeral instability. J Bone Joint Surg Am. 2003;85(5):878-84.
-
43Lansdown DA, Wang K, Bernardoni E, Frank RM, Yanke AB, Cole BJ, et al. Variability in the Contour of Cadaveric Anterior and Posterior Glenoids Based on Ipsilateral 3-Dimensional Computed Tomography Reconstructions: Implications for Clinical Estimation of Bone Loss. Arthroscopy. 2018;34(9):2560-6.
-
44Gyftopoulos S, Hasan S, Bencardino J, et al. Diagnostic accuracy of MRI in the measurement of glenoid bone loss. AJR Am J Roentgenol. 2012;199(4):873-8.
-
45Maio M, Sarmento M, Moira N, Cartucho A. How to measure a Hill–Sachs lesion: a systematic review. EFORT Open Rev. 2019;4(4):151-7.
-
46Stillwater L, Koenig J, Maycher B, Davidson M. 3D-MR vs. 3D-CT of the shoulder in patients with glenohumeral instability. Skeletal Radiol. 2017;46(3):325-31.
-
47Gyftopoulos S, Beltran LS, Bookman J, Rokito A. MRI Evaluation of Bipolar Bone Loss Using the On-Track Off-Track Method: A Feasibility Study. AJR Am J Roentgenol. 2015;205:848-52.
-
48Yamamoto N, Itoi E, Abe H, Minagawa H, Seki N, Shimada Y, Okada K. Contact between the glenoid and the humeral head in abduction, external rotation, and horizontal extension: a new concept of glenoid track. J Shoulder Elbow Surg. 2007;16:649-56.
-
49Huijsmans PE, Haen PS, Kidd M, Dhert WJ, van der Hulst VP, Willems WJ J. Quantification of a glenoid defect with three-dimensional computed tomography and magnetic resonance imaging: a cadaveric study. Shoulder Elbow Surg. 2007;16(6):803-9.
-
50Schneider AK, Hoy GA, Ek ET, et al. Interobserver and intraobserver variability of glenoid track measurements. J Shoulder Elbow Surg. 2017;26(4):573-9.
-
51Momaya AM, Tokish JM. Applying the Glenoid Track Concept in the Management of Patients with Anterior Shoulder Instability. Curr Rev Musculoskelet Med. 2017;10(4):463-8.
-
52Yamamoto N, Shinagawa K, Hatta T, Itoi E. Peripheral-Track and Central-Track Hill-Sachs Lesions: A New Concept of Assessing an On-Track Lesion. Am J Sports Med. 2020;48(1):33-8.
-
53Burkhart SS, Debeer JF, Tehrany AM, Parten PM. Quantifying glenoid bone loss arthroscopically in shoulder instability. Arthroscopy. 2002;18(5):488-91.
-
54Helfet AJ. Coracoid transplantation for recurring dislocation of the shoulder. J Bone Joint Surg Br. 1958;40:198-202.
-
55Mead NC, Sweeney HJ. Bristow procedure (letter). Spectator. 1964 July 9.
-
56Barth J, Boutsiadis A, Neyton L, Lafosse L, Walch G. Can a Drill Guide Improve the Coracoid Graft Placement During the Latarjet Procedure? A Prospective Comparative Study With the Freehand Technique. Orthop J. Sports Med. 2017;5(10):232596711773421.
-
57Lafosse L, Boyle S. Arthroscopic Latarjet procedure. J Shoulder Elbow Surg. 2010;19:2-12.
-
58Boileau P, Mercier N, Roussanne Y, Thelu CE, Old J. Arthroscopic Bankart-Bristow-Latarjet procedure: the development and early results of a safe and reproducible technique. Arthroscopy. 2010;11:1434-50.
-
59Latarjet M. A propos du traitement des luxations récidivants de l’épaule. Lyon Chir. 1954;49:994-1003.
-
60May VR. A modified Bristow operation for anterior recurrent dislocation of the shoulder. J Bone Joint Surg Am. 1970;52:1010-6.
-
61Patte D, Bernageau J, Bancel P. The anteroinferior vulnerable point of the glenoid rim. In: Bateman, Welsch (ed.). Surgery of the shoulder. New York: Marcel Dekker; 1985. pp. 94-9.
-
62De Beer JF, Roberts C. Glenoid bone defects–open latarjet with congruent arc modification. Orthop Clin North Am. 2010;41(3):407-15.
-
63Allain J, Goutallier D, Glorion C. Long-term results of the Latarjet procedure for the treatment of anterior instability of the shoulder. J Bone Joint Surg Am. 1998;80:841-52.
-
64Hovelius L, Sandström B, Olofsson A, Svensson O, Rahme H. The effect of capsular repair, bone block healing, and position on the results of the Bristow-Latarjet procedure (study III): long-term follow-up in 319 shoulders. J Should Elbow Surg. 2012;21(5):647-60.
-
65Cerciello S, Edwards TB, Walch G. Chronic anterior glenohumeral instability in soccer players: results for a series of 28 shoulders treated with the Latarjet procedure. J Orthop Traumatol. 2012;13(4):197-202.
-
66Neyton L, Young A, Dawidziak B, et al. Surgical treatment of anterior instability in rugby union players: clinical and radiographic results of the Latarjet-Patte procedure with minimum 5-year follow-up. J Shoulder Elbow Surg. 2012;21(12):1721-7.
-
67Hart R, Sváb P, Krejzla J. Modified Latarjet procedure for recurrent shoulder dislocation in elderly patients. Acta Chir Orthop Traumatol Cech. 2010;77(2):105-11.
-
68Schmid SL, Farshad M, Catanzaro S, Gerber C. The Latarjet procedure for the treatment of recurrence of anterior instability of the shoulder after operative repair: a retrospective case series of forty-nine consecutive patients. J Bone Joint Surg. 2012;94(11):e75.
-
69Boileau P, Mercier N, Roussanne Y, Thélu CÉ, Old J. Arthroscopic Bankart-Bristow-Latarjet procedure: the development and early results of a safe and reproducible technique. Arthroscopy. 2010;26(11):1434-50.
-
70Warner JJ, Gill TJ, O’Hollerhan JD, et al. Anatomical glenoid reconstruction for recurrent anterior glenohumeral instability with glenoid deficiency using an autogenous tricortical iliac crest bone graft. Am J Sports Med. 2006;34:205-12.
-
71Gebhard F, Dragees M, Steinmann R, Hoellen I, Hartel W. Functional outcome of Eden-Hybinette-Lange operation in post-traumatic recurrent shoulder dislocation. Der Unfallchirurg. 1997;100:770-5.
-
72Auffarth A, Schauer J, Matis N, et al. The J-bone graft for anatomical glenoid reconstruction in recurrent posttraumatic anterior shoulder dislocation. Am J Sports Med. 2008;36:638-47.
-
73Provencher MT, Frank RM, Golijanin P, et al. Distal Tibia Allograft Glenoid Reconstruction in Recurrent Anterior Shoulder Instability: Clinical and Radiographic Outcomes. Arthroscopy. 2017;33(5):891-7.
-
74Taverna E, D'Ambrosi R, Perfetti C, Garavaglia G. Arthroscopic bone graft procedure for anterior inferior glenohumeral instability. Arthrosc Tech. 2014;3:e653-e660.
-
75Boileau P, Duysens C, Saliken D, Lemmex DB, Bonnevialle N. All-arthroscopic, guided Eden-Hybbinette procedure using suture-button fixation for revision of failed Latarjet. J Shoulder Elbow Surg. 2019;28:e377-e388.
-
76Hachem AI, Del Carmen M, Verdalet I, Rius J. Arthroscopic Bone Block Cerclage: A Fixation Method for Glenoid Bone Loss Reconstruction Without Metal Implants. Arthrosc Tech. 2019;8(12):e1591-e1597.
-
77Zhao J, Huangfu X, Yang X, Xie G, Xu C. Arthroscopic glenoid bone grafting with nonrigid fixation for anterior shoulder instability: 52 patients with 2- to 5-year follow-up. Am J Sports Med. 2014;42:831-9.
-
78Whelan A, Coady C, Ho-Bun Wong I. Anterior glenohumeral capsular reconstruction using a human acellular dermal allograft. Arthrosc Tech. 2018;7:e1235-e1241.
-
79Regan Jr WD, Webster-Bogaert S, Hawkins RJ, Fowler PJ. Comparative functional analysis of the Bristow, Magnuson-Stack, and Putti-Platt procedures for recurrent dislocation of the shoulder. Am J Sports Med. 1989;17:42-8.
-
80Weber BG, Simpson LA, Hardegger F. Rotational humeral osteotomy for recurrent anterior dislocation of the shoulder associated with a large Hill-Sachs lesion. J Bone Joint Surg. 1984;66:1443-50.
-
81Saltzman BM, Riboh JC, Cole BJ, Yanke AB. Humeral Head Reconstruction With Osteochondral Allograft Transplantation. Arthroscopy. 2015;31(9):1827-34.
-
82Wolf EM, Pollack M, Smalley C. Hill-Sachs "Remplissage": an arthroscopic solution for the engaging Hill-Sachs lesion. Arthroscopy. 2007;23:e1-2.
-
83Kazel MD, Sekiya JK, Greene JA, Bruker CT. Percutaneous correction (humeroplasty) of humeral head defects (Hill-Sachs) associated with anterior shoulder instability: a cadaveric study. Arthroscopy. 2005;12:1473-8.
-
84Re P, Gallo RA, Richmond JC. Transhumeral head plasty for large Hill-Sachs lesions. Arthroscopy. 2006;22:e1-4.
-
85Connolly JF. Humeral head defects associated with shoulder dislocation: their diagnostic and surgical significance. Instr Course Lect. 1972;21:42-54.
-
86Purchase RJ, Wolf EM, Hobgood ER, Pollock ME, Smalley CC. Hill-Sachs "remplissage": an arthroscopic solution for the engaging hill-sachs lesion. Arthroscopy. 2008;24:723-6.
-
87Koo SS, Burkhart SS, Ochoa E. Arthroscopic double-pulley remplissage technique for engaging Hill-Sachs lesions in anterior shoulder instability repairs. Arthroscopy. 2009;25(11):1343-8.
-
88Nourissat G, Kilinc AS, Werther JR, Doursounian L. A prospective, comparative, radiological, and clinical study of the influence of the "remplissage" procedure on shoulder range of motion after stabilization by arthroscopic Bankart repair. Am J Sport Med. 2011;39(10):2147-52.
-
89Franceschi F, Papalia R, Rizzello G, et al. Remplissage repair-new frontiers in the prevention of recurrent shoulder instability: a 2-year follow-up comparative study. Am J Sports Med. 2012;40(11):2462-9.
-
90Elkinson I, Giles JW, Faber KJ, et al. The effect of the remplissage procedure on shoulder stability and range of motion: an in vitro biomechanical assessment. J Bone Joint Surg. 2012;94(11):1003-12.
-
91Boileau P, O'Shea K, Vargas P, et al. Anatomical and functional results after arthroscopic Hill-Sachs remplissage. J Bone Joint Surg. 2012;94(7):618-26.
-
92Balg F, Boileau P. The instability severity index score. A simple pre-operative score to select patients for arthroscopic or open shoulder stabilisation. J Bone Joint Surg Br. 2007;89:1470-7.
-
93Ruiz Ibán MA, Asenjo Gismero CV, Moros Marco S, et al. Instability severity index score values below 7 do not predict recurrence after arthroscopic Bankart repair. Knee Surg Sports Traumatol Arthrosc. 2019 Dec;27(12):3905-11.
-
94Di Giacomo G, Peebles LA, Pugliese M, et al. Glenoid Track Instability Management Score: Radiographic Modification of the Instability Severity Index Score. Arthroscopy. 2020;36(1):56-67.
-
95Yamamoto N, Itoi E, Abe H, et al. Effect of an anterior glenoid defect on anterior shoulder stability: a cadaveric study. Am J Sports Med. 2009;37:949-54.
-
96Abrams JS. Role of arthroscopy in treating anterior instability of the athlete’s shoulder. Sports Med Arthrosc. 2007;15:230-8.
-
97Plath JE, Henderson DJH, Coquay J, Dück K, Haeni D, Lafosse L. Does the arthroscopic Latarjet procedure effectively correct "off-track" Hill-Sachs lesions? Am J Sports Med. 2017:363546517728717.
-
98Miniaci A, Berlet G, Hand C, et al. Segmental humeral head allografts for recurrent anterior instability of the shoulder with large Hill-Sachs defects: a two to 8 year follow up. J Bone Joint Surg Br. 2008;90(suppl I):86.
-
99Purchase RJ, Wolf EM, Hob-Good ER, et al. Hill-Sachs ‘‘remplissage’’: an arthroscopic solution for the engaging Hill-Sachs lesion. Arthroscopy. 2008;24:723-6.
-
100Toro F, Melean P, Moraga C, et al. Remplissage: infraspinatus tenodesis and posterior capsulodesis for the treatment of Hill Sachs lesions: an all intraarticular technique. Tech Shoulder Elbow Surg. 2008;9:188-92.
-
101Bushnell BD, Creighton RA, Herring MM. Hybrid treatment of engaging Hill-Sachs lesions: arthroscopic capsulolabral repair and limited posterior approach for bone grafting. Tech Shoulder Elbow Surg. 2007;8:194-203.
Descargar artículo:
Licencia:
Este contenido es de acceso abierto (Open-Access) y se ha distribuido bajo los términos de la licencia Creative Commons CC BY-NC-ND (Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional) que permite usar, distribuir y reproducir en cualquier medio siempre que se citen a los autores y no se utilice para fines comerciales ni para hacer obras derivadas.
Comparte este contenido
En esta edición
- No olvidarse de recordar
- Estudio anatómico sobre artrodesis subtalar: portales anterolaterales vs. posteriores
- Guías personalizadas impresas en 3D para la reparación de las roturas de la raíz posterior del menisco interno. Resultados preliminares
- La reconstrucción ligamentosa anatómica con aloinjerto en luxaciones acromioclaviculares crónicas restaura la estabilidad articular y permite recuperar la función. Resultados a corto plazo en 14 casos
- Tendinopatía rotuliana: enfoque diagnóstico y escalas de valoración funcional
- Manejo actual de las roturas del ligamento cruzado posterior. Una revisión narrativa
- Manejo de la inestabilidad anterior de hombro con defectos óseos
- Técnica quirúrgica de reconstrucción anatómica abierta con aloinjerto para el tratamiento de las luxaciones acromioclaviculares crónicas
- Lesión simultánea pero diferente de ambas raíces meniscales posteriores con lesión multiligamentosa de rodilla tras traumatismo de alta energía. Presentación de un caso
- Sinovitis vellonodular pigmentada de tobillo
Más en PUBMED
Más en Google Scholar
Más en ORCID


Revista Española de Artroscopia y Cirugía Articular está distribuida bajo una licencia de Creative Commons Reconocimiento-NoComercial-SinObraDerivada 4.0 Internacional.